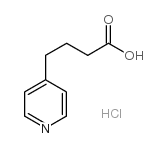
4-(Pyridin-4-yl)butansäurehydrochlorid
- CAS-Nr.71879-56-6
- QualitätIndustrie / Pharma
- Verfügbarkeit● Auf Lager
Hochreines pharmazeutisches Zwischenprodukt zur Synthese von Tirofiban-Hydrochlorid. Lieferbar in Industriemengen unter strenger Qualitätskontrolle.
Angebot anfordernTechnische Produktdetails
Produktübersicht
4-(Pyridin-4-yl)butansäurehydrochlorid ist eine spezielle organische Verbindung, die für ihre kritische Rolle in der modernen Pharmasynthese bekannt ist. Als wesentlicher Baustein dient diese Substanz als unverzichtbarer Vorläufer bei der Herstellung fortschrittlicher kardiovaskulärer Therapeutika. Unsere Anlage produziert dieses Zwischenprodukt unter strengen Qualitätsmanagementsystemen, um Konsistenz und Zuverlässigkeit für nachgelagerte pharmazeutische Anwendungen zu gewährleisten.
Die chemische Struktur umfasst einen Pyridinring, gebunden an eine Butansäurekette, stabilisiert als Hydrochloridsalz. Diese Konfiguration verbessert Stabilität und Löslichkeit während verschiedener Synthesereaktionen. Wir priorisieren hohe Reinheitsgrade, um Verunreinigungen zu minimieren, welche die Wirksamkeit des finalen Wirkstoffs beeinträchtigen könnten.
Technische Spezifikationen
| Parameter | Wert |
|---|---|
| Chemischer Name | 4-(Pyridin-4-yl)butansäurehydrochlorid |
| CAS-Nummer | 71879-56-6 |
| Summenformel | C9H12ClNO2 |
| Molekulargewicht | 201.65 |
| Erscheinungsbild | Weißes Pulver |
| Reinheit | ≥95% |
| Verunreinigungsgrad | ≤0.02% |
Industrielle Anwendungen
Diese Verbindung findet vorwiegend Verwendung als pharmazeutisches Zwischenprodukt in der Synthese von Tirofiban-Hydrochlorid. Tirofiban ist ein bekanntes Thrombozytenaggregationshemmer-Medikament zur Prävention thrombotischer kardiovaskulärer Ereignisse. Die Präzision der Zwischenstufe beeinflusst direkt das Qualitäts- und Sicherheitsprofil des finalen Arzneimittels.
- Primärer Vorläufer für die Synthese von Thrombozytenaggregationshemmern
- Einsatz in komplexen organischen Kupplungsreaktionen
- Unterstützt die pharmazeutische Großproduktion
- Kompatibel mit standardisierten GMP-Produktionslinien
Qualitätssicherung und Lagerung
Wir halten strenge Qualitätskontrollprotokolle während des gesamten Produktionsprozesses ein. Jede Charge durchläuft umfassende Tests mittels Hochleistungsflüssigkeitschromatographie und weiterer analytischer Methoden zur Verifizierung von Identität und Reinheit. Ein Analysezertifikat (CoA) wird jeder Sendung beigefügt, um Transparenz und Konformität zu gewährleisten.
Eine sachgemäße Lagerung ist essenziell, um die Stabilität dieses Hydrochloridsalzes zu erhalten. Das Produkt sollte kühl und trocken gelagert werden, idealerweise zwischen 2-8°C. Behälter müssen dicht verschlossen sein, um vor Feuchtigkeit und starkem Licht zu schützen. Wir bieten flexible Verpackungsoptionen, einschließlich 25-kg-Kartonfässer, maßgeschneidert für spezifische logistische Anforderungen im globalen Vertrieb.