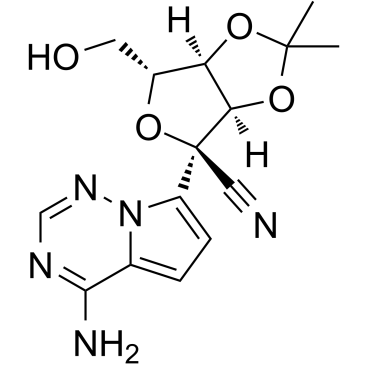
Impureza O-Desfosfato Acetonido de Remdesivir
- No. CAS1191237-80-5
- GradoIndustrial / Farmacéutico
- Disponibilidad● En Stock
Impureza de Remdesivir O-Desfosfato Acetonido de alta pureza (CAS 1191237-80-5), diseñada para investigación farmacéutica y validación de métodos analíticos. Calidad certificada con COA completo.
Solicitar CotizaciónDetalles Técnicos
Descripción General del Producto
Nuestra Impureza O-Desfosfato Acetonido de Remdesivir es un estándar de referencia crítico e intermedio utilizado extensivamente en el sector de investigación y desarrollo farmacéutico. Este compuesto sirve como un análogo estructural clave asociado con la vía de síntesis de Remdesivir, un análogo de nucleósido notable investigado para aplicaciones antivirales.
Como intermedio químico especializado, juega un papel indispensable en el perfilado de impurezas, la validación de métodos y los procesos de control de calidad dentro de entornos de laboratorio regulados. Entendemos los requisitos estrictos del análisis farmacéutico moderno.
Por lo tanto, este producto se fabrica bajo sistemas de gestión de calidad estrictos para garantizar consistencia y fiabilidad. Está destinado estrictamente para uso en investigación y desarrollo por profesionales calificados en entornos industriales o académicos. Nuestro compromiso con la excelencia asegura que cada lote cumpla con los más altos estándares de pureza química e integridad estructural requeridos para resultados analíticos precisos.
Propiedades Químicas y Estructura
La estructura química de esta impureza presenta un sistema heterocíclico complejo caracterizado por un núcleo pirrolo-triazina unido a un moiety de azúcar modificado. Específicamente, la molécula contiene un grupo protector acetonido y una funcionalidad nitrilo, cruciales para su estabilidad y reactividad durante las transformaciones sintéticas.
La estereoquímica se controla meticulosamente, con configuraciones específicas en múltiples centros quirales. Esto asegura que el material refleje con precisión el perfil de impurezas objetivo encontrado en las sustancias farmacéuticas finales. Entender las propiedades fisicoquímicas de este intermedio es vital para los investigadores que desarrollan métodos analíticos robustos.
El compuesto exhibe características de solubilidad y perfiles de estabilidad específicos que deben considerarse durante el almacenamiento y manipulación. El manejo adecuado asegura que el material permanezca estable con el tiempo, preservando su utilidad como estándar de referencia fiable para cromatografía líquida de alta resolución (HPLC) y otras técnicas espectroscópicas.
Especificaciones de Calidad
La aseguramiento de calidad es la piedra angular de nuestro proceso de fabricación. Cada lote se somete a pruebas rigurosas utilizando instrumentación analítica avanzada para verificar identidad, pureza y composición estereoquímica.
Nos adherimos a las directrices internacionales para estándares de impurezas, asegurando que nuestros productos respalden presentaciones regulatorias y auditorías de calidad internas. La siguiente tabla describe las especificaciones típicas para este material:
| Parámetros de Análisis | Especificación | Resultados |
|---|---|---|
| Aspecto | Sólido blanco | Conforme |
| Identificación | HPLC | Conforme |
| Pureza (HPLC) | ≥98.0% | 99.6% |
| Exceso Enantiomérico | ≥98.0% | 99.2% |
| Conclusión | Conforme al Estándar de Fábrica | |
Aplicaciones Industriales
Este intermedio se utiliza principalmente en el desarrollo y validación de métodos analíticos para productos farmacéuticos antivirales. Los investigadores emplean este material para spiked samples, calibrar instrumentos y establecer límites de detección para pruebas de impurezas.
Adicionalmente, sirve como una herramienta valiosa para estudiar vías de degradación y métodos indicadores de estabilidad. Al utilizar estándares de impurezas de alta calidad, las compañías farmacéuticas pueden asegurar la seguridad y eficacia de sus productos finales mediante un control de calidad exhaustivo.
- Perfilado e identificación de impurezas en el análisis de sustancias farmacéuticas.
- Validación de métodos cromatográficos para cumplimiento regulatorio.
- Investigación sobre rutas sintéticas y optimización de procesos.
- Estudios de estabilidad y caracterización de productos de degradación.
Embalaje y Almacenamiento
Para mantener la integridad de la estructura química, este producto se envasa en contenedores sellados bajo condiciones de atmósfera inerte cuando es necesario. Recomendamos almacenar el material en un lugar fresco y seco, lejos de la luz directa y la humedad.
Las condiciones de almacenamiento adecuadas son esenciales para prevenir la hidrólisis u otras reacciones de degradación que podrían comprometer la pureza del estándar. Cada envío incluye un Certificado de Análisis (COA) completo que detalla los resultados de pruebas específicos para ese lote, asegurando total trazabilidad y transparencia para nuestros clientes globales.



