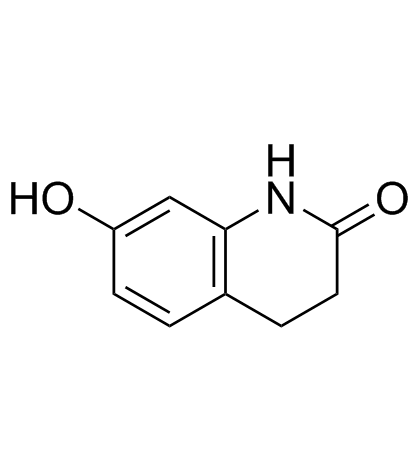
7-Hydroxy-3,4-dihydro-1H-quinolin-2-one
- CAS-Nr.22246-18-0
- QualitätIndustrie / Pharma
- Verfügbarkeit● Auf Lager
Hochreine pharmazeutische Zwischenstufe zur Synthese von Aripiprazol. Verfügbar in Großmengen mit vollständiger Chargendokumentation (CoA) und weltweitem Versand.
Angebot anfordernTechnische Produktdetails
Produktübersicht
Hier präsentieren wir das detaillierte Profil für 7-Hydroxy-3,4-dihydro-1H-quinolin-2-one. Diese spezielle pharmazeutische Zwischenstufe übernimmt eine Schlüsselrolle bei der Synthese moderner Therapeutika. Identifiziert unter der CAS-Nummer 22246-18-0, wird diese Verbindung präzise gefertigt, um den strengen Anforderungen der globalen Pharmaindustrie gerecht zu werden. Unsere Produktionsstätten arbeiten nach strikten Qualitätsmanagementsystemen. So gewährleisten wir, dass jede Charge konsistente Leistung und Zuverlässigkeit für Ihre Weiterverarbeitung bietet. Wir kennen die Bedeutung einer unterbrechungsfreien Lieferkette in der Arzneimittelproduktion und halten strategische Lagerbestände zur Unterstützung unserer Partner vor.
Technische Daten
| Parameter | Wert |
|---|---|
| Chemische Bezeichnung | 7-Hydroxy-3,4-dihydro-1H-quinolin-2-one |
| CAS-Nummer | 22246-18-0 |
| Summenformel | C9H9NO2 |
| Molare Masse | 163.173 |
| Erscheinungsbild | Off-white Pulver |
| Gehalt | ≥98.0% |
| Schmelzpunkt | 232-237°C |
| Trocknungsverlust | ≤0.5% |
| Glührückstand | ≤1.0% |
| Gesamtverunreinigungen | ≤1.0% |
Industrielle Anwendungen
Die Hauptanwendung dieser chemischen Einheit liegt in der Funktion als entscheidender Baustein für die Synthese von Aripiprazol, einem weit verbreiteten atypischen Antipsychotikum. Die Präzision dieses Synthesewegs erfordert Zwischenprodukte von außergewöhnlicher Qualität, um Sicherheit und Wirksamkeit des fertigen Arzneimittels zu garantieren. Durch den Einsatz unseres klassifizierten Materials können Pharmahersteller ihre regulatorischen Zulassungsdossiers optimieren und die Produktsicherheit gewährleisten. Wir unterstützen unsere Kunden mit vollständiger Dokumentation, einschließlich Prüfzertifikaten (CoA) und Methodenvalidierungsberichten. Dies erleichtert Auditprozesse und sichert die Compliance mit internationalen Standards wie GMP und ISO.
Qualitätskontrolle und Prüfung
Die Einhaltung hoher Reinheitsgrade ist essenziell, um Nebenreaktionen bei der Herstellung von pharmazeutischen Wirkstoffen (APIs) zu verhindern. Unser technisches Team fokussiert sich auf die Optimierung von Kristallisations- und Reinigungsprozessen zur Minimierung von Verunreinigungen. Diese Sorgfalt garantiert, dass das Material in Reaktionsgefäßen vorhersagbar performt, Abfall reduziert und die Gesamtausbeute für unsere Partner verbessert. Jede Charge durchläuft rigorose Tests mittels fortschrittlicher Analyseverfahren wie HPLC und NMR, um strukturelle Integrität und Reinheitsprofile zu verifizieren. Wir verpflichten uns zu Transparenz und liefern detaillierte Testergebnisse mit jeder Sendung.
Lagerung und Logistik
Lagerung und Handling erfordern Standardvorkehrungen für feine chemische Pulver. Das Material ist kühl und belüftet zu lagern, geschützt vor direkter Sonneneinstrahlung und Feuchtigkeit. Eine ordnungsgemäße Versiegelung ist entscheidend für die Stabilität über längere Zeiträume. Wir bieten flexible Verpackungslösungen an, typischerweise in 25-kg-Fässern, passen uns jedoch gerne spezifischen logistischen Anforderungen an. Unser globales Versandnetzwerk sichert pünktliche Lieferung an wichtige Pharma-Standorte in Asien, Europa und Amerika. Wir arbeiten mit verlässlichen Logistikpartnern zusammen, um den sicheren und konformen Transport aller Chemikalien zu gewährleisten.
Ihre Vorteile bei unserer Lieferung
- Chargekonstante Reproduzierbarkeit für verlässliche Produktionsskalierung.
- Wettbewerbsfähige Konditionen für Großmengen und Langzeitpartnerschaften.
- Persönlicher technischer Support zur Syntheseoptimierung.
- Verlässliche Produktionsplanung zur Vermeidung von Lieferengpässen.
- Verpflichtung zu Sicherheit und Umweltverantwortung in der Fertigung.



