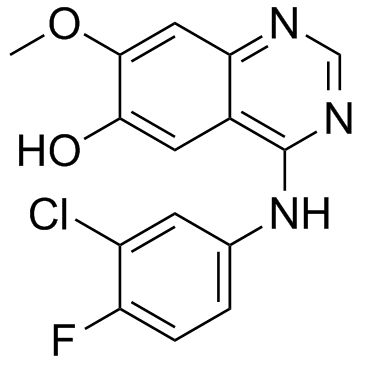
O-Desmorpholinopropyl Gefitinib
- No. CAS184475-71-6
- GradoIndustrial / Farmacéutico
- Disponibilidad● En Stock
Intermedio farmacéutico de alta pureza, esencial para la síntesis de Gefitinib. Ofrece estabilidad superior y calidad consistente para la fabricación global de API.
Solicitar CotizaciónDetalles Técnicos
Descripción General del Producto
El O-Desmorpholinopropyl Gefitinib actúa como un precursor estructural crítico en la industria farmacéutica, diseñado específicamente para la síntesis de inhibidores de tirosina quinasa avanzados. Este derivado de quinazolina representa un bloque de construcción clave en la cadena de producción para terapias oncológicas dirigidas. Nuestro proceso de fabricación asegura que cada lote cumpla con rigurosos estándares internacionales, brindando confiabilidad para la producción de API posterior.
Como intermedio especializado, este compuesto presenta una estructura química robusta que facilita reacciones de acoplamiento eficientes. La arquitectura molecular precisa permite una integración perfecta en rutas de síntesis complejas, minimizando reacciones secundarias y maximizando el rendimiento global. Priorizamos la consistencia en cada corrida de producción para apoyar los requisitos de fabricación farmacéutica a gran escala.
Especificaciones Técnicas
El control de calidad es primordial en el suministro de intermedios farmacéuticos. Nuestra instalación utiliza métodos analíticos avanzados para verificar identidad y pureza. La siguiente tabla describe los parámetros físicos y químicos estándar garantizados para este producto.
| Parámetro | Especificación |
|---|---|
| Número CAS | 184475-71-6 |
| Fórmula Molecular | C15H11ClFN3O2 |
| Peso Molecular | 319.72 g/mol |
| Apariencia | Polvo marrón pálido |
| Pureza (HPLC) | ≥98.5% |
| Pérdida por secado | ≤1.0% |
| Residuo de ignición | ≤0.1% |
| Punto de fusión | 260ºC |
Aplicaciones Industriales
Este intermedio se utiliza principalmente en la investigación y desarrollo de inhibidores del receptor del factor de crecimiento epidérmico (EGFR). Las compañías farmacéuticas dependen de precursores de alta calidad para asegurar la seguridad y eficacia del ingrediente farmacéutico activo final. La estabilidad del compuesto bajo condiciones estándar de almacenamiento lo hace idóneo para logística global y cronogramas de producción extendidos.
Más allá de la síntesis estándar, este material soporta estudios de optimización de procesos. Los químicos usan este intermedio para refinar condiciones de reacción, mejorar la escalabilidad y reducir costos de fabricación. Nuestro equipo técnico brinda soporte integral para ayudar a los clientes a integrar este material en su flujo de trabajo específico eficientemente.
Garantía de Calidad y Almacenamiento
Cumplimos con estrictos sistemas de gestión de calidad para mantener la integridad del producto. Cada envío viene acompañado de un Certificado de Análisis (COA) que detalla los resultados de pruebas específicos del lote. El almacenamiento adecuado es esencial para mantener la estabilidad química en el tiempo. Recomendamos mantener el material en un ambiente fresco y ventilado, lejos de la luz solar directa y la humedad.
Las opciones de embalaje son flexibles para satisfacer las necesidades diversas de los clientes. Los tambores de exportación estándar aseguran la seguridad durante el tránsito, mientras que el embalaje personalizado está disponible bajo solicitud. Nuestras capacidades de cadena de suministro global aseguran una entrega oportuna a centros de investigación e instalaciones de fabricación en todo el mundo, apoyando la producción continua sin interrupciones.



