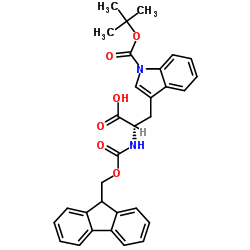
Fmoc-L-Trp(Boc)-OH
- CAS-Nr.143824-78-6
- QualitätIndustrie / Pharma
- Verfügbarkeit● Auf Lager
Hochreines Fmoc-L-Trp(Boc)-OH (CAS 143824-78-6) stellt ein essenzielles, geschütztes Tryptophan-Derivat für die Festphasenpeptidsynthese dar. Es garantiert regioselektiven Schutz sowie eine hervorragende Kupplungseffizienz.
Angebot anfordernTechnische Produktdetails
Produktübersicht
Fmoc-L-Trp(Boc)-OH, chemisch bezeichnet als (2S)-2-(9H-fluoren-9-ylmethoxycarbonylamino)-3-[1-[(2-methylpropan-2-yl)oxycarbonyl]indol-3-yl]propansäure, ist ein doppelt geschütztes L-Tryptophan-Derivat. Es findet breite Anwendung in der modernen Peptidsynthese. Dieser Baustein verfügt über eine orthogonale Schutzgruppenstrategie: Die α-Aminogruppe ist durch die basenlabile 9-Fluorenylmethoxycarbonyl (Fmoc)-Einheit geschützt. Gleichzeitig ist der Indol-Stickstoff mit einer säurelabilen tert-Butyloxycarbonyl (Boc)-Gruppe geschützt. Dieses strategische Design ermöglicht eine präzise, schrittweise Elongation in der Festphasenpeptidsynthese (SPPS). Nebenreaktionen am empfindlichen Indolring werden somit vermieden.
Spezifikationen
| Summenformel | C31H30N2O6 |
|---|---|
| Molekulargewicht | 526.58 g/mol |
| CAS-Nummer | 143824-78-6 |
| Erscheinungsbild | Weißes bis cremefarbenes kristallines Pulver |
| Reinheit (HPLC) | ≥99.0% |
| Optische Drehung | -19.0° ± 2.0° (c=1, DMF) |
| Wassergehalt | ≤0.50% |
| Schmelzpunkt | 86–90°C |
| Löslichkeit | Frei löslich in DMF, DMSO; schwer löslich in Wasser |
Industrielle Anwendungen
Als spezialisierter Aminosäure-Baustein ist Fmoc-L-Trp(Boc)-OH unverzichtbar für die Synthese komplexer therapeutischer Peptide mit Tryptophan-Resten. Der Haupteinsatzbereich liegt in der Forschung sowie der GMP-konformen Herstellung peptidbasierter Pharmazeutika. Der Indolschutz verhindert hierbei Alkylierungen oder Oxidationen während des Kettenaufbaus. Zu den Hauptanwendungsgebieten zählen:
- Festphasensynthese bioaktiver Peptide für die Onkologie- und Endokrinologieforschung
- Produktion von Peptid-Wirkstoffen (APIs) mit hoher enantiomerer Reinheit
- Entwicklung von Peptidbibliotheken für das Screening zur Wirkstoffentwicklung
- Kundenspezifische Synthese modifizierter tryptophanhaltiger Sequenzen
Bei Lagerung zwischen 2–8°C in einem dicht verschlossenen Behälter unter trockenen, inerten Bedingungen bewahrt dieses Reagenz seine Stabilität und Leistungsfähigkeit über längere Zeiträume. Eine rigorose Qualitätskontrolle stellt die Einhaltung internationaler pharmakopöischer Standards bezüglich Restlösungsmitteln, Verunreinigungen und enantiomerer Reinheit sicher.